În calitate de furnizor de încredere de 3 - hexanonă, am asistat la un interes din ce în ce mai mare pentru înțelegerea reacțiilor sale chimice, în special cu halogeni. Această postare de blog își propune să ofere o perspectivă cuprinzătoare asupra modului în care 3 - hexanona reacționează cu halogenii, explorând mecanismele de bază, produsele formate și implicațiile practice.
Structura chimică și reactivitatea 3-hexanonei
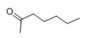
Înainte de a explora reacțiile cu halogenii, este esențial să înțelegem structura chimică a 3 - hexanonei. Formula sa moleculară este C₆H₁₂O și aparține familiei cetonelor. Gruparea carbonil (C = O) din 3 - hexanonă este o grupare funcțională cheie care conferă reactivitate unică. Carbonul carbonil este electrofil datorită diferenței de electronegativitate dintre carbon și oxigen, în timp ce alfa - hidrogenii (hidrogenii de pe atomii de carbon adiacenți grupului carbonil) sunt relativ acizi.
Mecanisme generale de reacție a cetonelor cu halogeni
Cetonele pot reacționa cu halogenii prin două mecanisme principale: halogenarea acidă - catalizată și bazică - catalizată.
Acid - Halogenare catalizată
În halogenarea catalizată cu acid, reacția are loc de obicei în prezența unui catalizator acid, cum ar fi acidul acetic. Primul pas implică protonarea oxigenului carbonil de către acid. Această protonare crește electrofilitatea carbonilului, făcându-l mai susceptibil la atacul halogenului.
Alfa - hidrogenii cetonei sunt apoi extrași de o bază (de obicei baza conjugată a catalizatorului acid), formând un intermediar enol. Intermediarul enol este o structură stabilizată prin rezonanță cu o legătură dublă între carbonul alfa și carbonul carbonil. Enolul reacţionează apoi cu halogenul, rezultând înlocuirea unui alfa - hidrogen cu un atom de halogen.
Reacția poate continua, ducând la halogenări multiple la pozițiile alfa. Cu toate acestea, rata halogenărilor ulterioare scade deoarece efectul de retragere de electroni al halogenului face ca alfa-hidrogenii rămași să fie mai puțin acizi, iar intermediarul enol mai puțin stabil.
Baza - Halogenare catalizata
Baza - halogenarea catalizata are loc in prezenta unei baze, cum ar fi ionii de hidroxid. Baza extrage un alfa - hidrogen din cetonă, formând un ion enolat. Ionul enolat este un nucleofil puternic și reacționează ușor cu halogenul.
Spre deosebire de halogenarea catalizată acid, halogenarea catalizată de bază duce adesea la halogenarea completă a tuturor hidrogenilor alfa de pe același atom de carbon. Acest lucru se datorează faptului că efectul de retragere de electroni al halogenului nu afectează semnificativ formarea ionului enolat în mecanismul catalizat de bază. În unele cazuri, dacă cetona are trei alfa - hidrogeni pe același atom de carbon, reacția poate continua pentru a forma o trihalometil cetona. Această trihalometil cetonă poate suferi apoi o reacție de scindare în prezența unei baze, rezultând formarea unui ion carboxilat și a unui haloform. Această reacție este cunoscută sub numele de reacție haloformă.
Reacția 3-hexanonei cu halogeni
Reacția cu clorul
Atunci când 3 - hexanona reacţionează cu clorul în prezenţa unui catalizator acid, intră în joc mecanismul de halogenare catalizat acid. Mai întâi are loc protonarea oxigenului carbonil, urmată de formarea unui intermediar enol. Enolul reacţionează apoi cu clorul, înlocuind un alfa - hidrogen cu un atom de clor.
Dacă reacția este efectuată în condiții catalizate de bază, baza extrage un alfa - hidrogen pentru a forma un ion enolat. Ionul enolat reacționează cu clorul și, în funcție de condițiile de reacție, pot apărea multiple clorări în pozițiile alfa.
Produșii reacției cu clorul pot avea diferite aplicații. Cetonele clorurate sunt adesea folosite ca intermediari în sinteza produselor farmaceutice, agrochimice și a altor substanțe chimice fine. De exemplu, pot fi utilizați la prepararea compușilor cu proprietăți antibacteriene sau antifungice.
Reacția cu brom
Reacția 3-hexanonei cu bromul este similară cu cea cu clorul. În bromurarea catalizată acid, protonarea oxigenului carbonil este urmată de formarea unui intermediar enol, care reacţionează apoi cu bromul.
Bromurarea catalizată de bază are loc și prin formarea unui ion enolat. Cetonele bromurate sunt elemente de bază valoroase în sinteza organică. Ele pot fi folosite la prepararea coloranților, parfumurilor și a altor substanțe chimice de specialitate. Atomul de brom poate fi în continuare substituit sau reacţionat cu alţi reactivi pentru a introduce noi grupări funcţionale în moleculă.
Reacția cu iod
Reacția 3-hexanonei cu iodul este în general mai lentă în comparație cu clorul și bromul. Acest lucru se datorează faptului că iodul este mai puțin reactiv ca electrofil. Cu toate acestea, în prezența unei baze puternice sau în anumite condiții de reacție, iodul poate reacționa în continuare cu 3 - hexanona.
Mecanismele de reacție sunt similare cu cele cu clor și brom. În reacțiile catalizate de bază, ionul enolat format din 3-hexanona poate reacționa cu iodul, ducând la înlocuirea hidrogenului alfa cu atomi de iod. Cetonele iodate sunt de interes în domeniul radiofarmaceutic, unde compușii care conțin iod pot fi utilizați în scopuri imagistice și terapeutice.
Aplicații practice și semnificație
Reacțiile 3-hexanonei cu halogenii au aplicații practice semnificative. Produsele halogenate pot fi utilizate ca materii prime pentru sinteza unei game largi de compuși organici.
În industria farmaceutică, cetonele halogenate derivate din 3 - hexanonă pot fi utilizate în sinteza medicamentelor. De exemplu, ei pot fi utilizați la prepararea compușilor care vizează căi sau receptori biologici specifici. Prezența atomilor de halogen în acești compuși le poate îmbunătăți activitatea biologică, solubilitatea sau stabilitatea metabolică.
În industria agrochimică, cetonele halogenate pot fi utilizate în sinteza pesticidelor și erbicidelor. Atomii de halogen pot îmbunătăți eficacitatea acestor compuși prin creșterea afinității lor de legare la locurile țintă ale dăunătorilor sau buruienilor.
Comparație cu alți compuși similari
Este interesant să comparăm reactivitatea 3 - hexanonei cu alte cetone similare, cum ar fi4 - heptanonă,N - acid valeric, șiPinacolone.
4 - heptanona, care are o structură asemănătoare cu 3 - hexanona dar cu un lanț de carbon mai lung, suferă și reacții de halogenare catalizate acid și bazic. Mecanismele de reacție sunt similare, dar proprietățile fizice și chimice ale produselor pot diferi din cauza lanțului de carbon mai lung.
N - Acidul Valeric este un acid carboxilic, iar reactivitatea sa cu halogenii este diferită de cea a 3 - hexanonei. Acizii carboxilici reacționează de obicei cu halogenii în prezența unui catalizator pentru a forma halogenuri de acil, care este un tip diferit de reacție în comparație cu alfa - halogenarea cetonelor.
Pinacolone are o structură unică cu un carbon cuaternar adiacent grupării carbonil. Această structură își afectează reactivitatea cu halogenii. Prezența carbonului cuaternar face alfa-hidrogenii mai puțin acizi, iar mecanismele de reacție pot fi diferite de cele ale 3-hexanonei.
Concluzie
În concluzie, reacțiile 3-hexanonei cu halogenii sunt procese complexe, dar bine înțelese. Mecanismele catalizate acid și bazic conduc la formarea de produse halogenate cu aplicații variate în diferite industrii.


În calitate de furnizor de 3 - hexanonă, înțeleg importanța furnizării de produse de înaltă calitate pentru aceste reacții chimice. Dacă sunteți interesat să utilizați 3 - hexanona pentru aplicațiile dumneavoastră specifice sau aveți întrebări despre reacțiile sale cu halogenii, vă încurajez să mă contactați pentru discuții suplimentare și potențiale achiziții. Putem lucra împreună pentru a ne asigura că aveți cantitatea și calitatea potrivite de 3 - hexanonă pentru proiectele dumneavoastră.
Referințe
- March, J. (1992). Chimie organică avansată: reacții, mecanisme și structură (ed. a IV-a). Wiley - Interștiință.
- Carey, FA și Sundberg, RJ (2007). Chimie organică avansată: Partea A: Structură și mecanisme (ed. a 5-a). Springer.
- McMurry, J. (2012). Chimie organică (ed. a 8-a). Brooks/Cole.